В США отзывают дecятки пapтий лeкapcтв для сердечников: в аптеках уже дефицит
За последние шесть месяцев Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) отозвало десятки партий лекарств, которые выписывают для лечения высокого кровяного давления. Причиной стали опасения, что они могут быть заражены канцерогенным химическим веществом.

Фото: Depositphotos
В пятницу FDA заявило, что в настоящее время в стране не хватает часто назначаемого лекарства «Валсартан», но и другие медикаменты, применяемые при лечении высокого кровяного давления, могут также стать дефицитными из-за продолжающихся отзывов.
Было обнаружено, что некоторые общие препараты «Валсартана», продаваемые в США, загрязнены химическим веществом NDMA, которое связывают с раком.
«В целом, риск для отдельных пациентов остается очень небольшим, хотя это не уменьшает значимость этого эпизода или наших опасений», — заявил комиссар FDA доктор Скотт Готтлиб и доктор Джанет Вудкок, директор Центра оценки и исследования лекарственных средств.
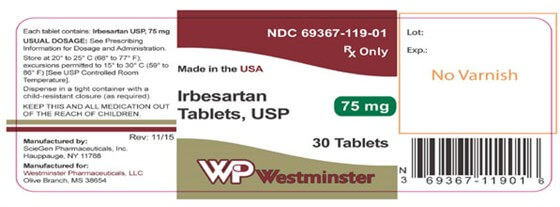
Фото: FDA
Самый последний отзыв произошел 18 января, когда Prinston Pharmaceuticals объявила о добровольном отзыве одной партии таблеток «Ирбесартана» и семи партий таблеток «Ирбесартана HCTZ», обычного лекарства от кровяного давления.
Большинство идентифицированных партий были заражены NDEA или NDMA, N-нитрозодиметиламина, которые FDA классифицировал как «вероятный канцероген для человека». Эти загрязнители окружающей среды также содержатся в воде и пищевых продуктах, включая мясо, молочные продукты и овощи,
Загрязненные лекарства были обнаружены на фабриках в Китае, которые производят ингредиенты «Валсартана» и отправляют их компаниям-генерикам по всему миру.
Летом 2018 года FDA предупредило китайскую компанию Zhejiang Huahai Pharmaceutical Co. о том, что некоторые лекарственные препараты, содержащие «Валсартан», содержат примеси NDMA и представляют потенциальную угрозу безопасности. FDA выпустило предупреждающее письмо для компании, в котором сообщалось о нескольких нарушениях производства, включая контроль примесей и перекрестное загрязнение от одной производственной линии к другой.
«Компании знали, что у них есть проблема, но не решали ее в течение шести лет, — сказала Розмари Гибсон, эксперт по здравоохранению в Центре Гастингса и автор книги «China Rx: выявление рисков зависимости Америки от Китая». — Это не случайность, это была известная серьезная проблема. Эта компания выпускала опасный продукт для людей».
Представитель FDA сказал NBC News, что агентство не может предсказать, как долго будут продолжаться отзывы.
В 2016 году было выписано около 14 миллионов назначений на «Валсартан» или препарат, который его включает. Еще 3,6 миллиона назначений были написаны на «Ирбесартан» в этом году.
По словам представителей фармацевтических компаний, о побочных эффектах не сообщалось, но эксперты считают, что зарубежные компании могут минимизировать риски для здоровья.
«Основной производитель, о котором идет речь, имел более чем 200-кратный допустимый уровень NDMA на таблетку, — сказал Гибсон в интервью NBC News. — Это было намного выше уровня, который FDA обнаружил в других продуктах «Валсартана»».
У FDA есть полный список лекарств, которые можно проверить.
FDA предлагает вернуть лекарства из списка в аптеку или врачу, который их выдал. Поскольку не все партии препаратов «Лозартана», «Валсартана» или «Ирбесартана» участвуют в отзыве, пациенты могут перейти на версию, сделанную другой компанией.
Насколько серьезен риск рака
FDA, которая проверяет все лекарственные препараты от иностранных заводов для использования в США, говорит, что риск очень низок. Тем не менее, FDA также отмечает, что уровни NDEA или NDMA, вызывающих рак агентов, содержащихся в образцах, находятся на недопустимых уровнях.
Поскольку прекращение приема сердечных препаратов представляет больший риск, чем зараженные лекарства в краткосрочной перспективе, врачи советуют пациентам продолжать принимать лекарства от кровяного давления до тех пор, пока не будет назначена замена, даже если этот препарат включен в отзыв.
Поскольку FDA исследует производственный процесс, который привел к загрязнению, Гибсон ожидает больше отзывов препарата от кровяного давления.
«Это всего лишь верхушка айсберга», — сказала она.
Читайте также на ForumDaily:
Где покупать доступные лекарства в США
Что я узнала о медицине в США, когда у меня появилась страховка
«Умные» лекарства: за что офисные работники полюбили модафинил
Личный опыт: как и кого лечат в Америке
Подписывайтесь на ForumDaily в Google NewsХотите больше важных и интересных новостей о жизни в США и иммиграции в Америку? — Поддержите нас донатом! А еще подписывайтесь на нашу страницу в Facebook. Выбирайте опцию «Приоритет в показе» — и читайте нас первыми. Кроме того, не забудьте оформить подписку на наш канал в Telegram и в Instagram— там много интересного. И присоединяйтесь к тысячам читателей ForumDaily New York — там вас ждет масса интересной и позитивной информации о жизни в мегаполисе.





















